Kulepakning er en pakking, eller stabling, av like store kuler. Krystallstrukturen av mange metaller kan beskrives som en effektiv pakking av slike kuler.
Et sett av like store kuler som er pakket tett sammen i et plan, vil ligge som i figuren. Hver kule er omgitt av seks andre kuler i like stor avstand. Legger man en kule oppå, som også vist i figuren, vil den ligge mellom tre andre kuler. Avstanden til dem er som avstanden til de seks andre kulene i samme plan.
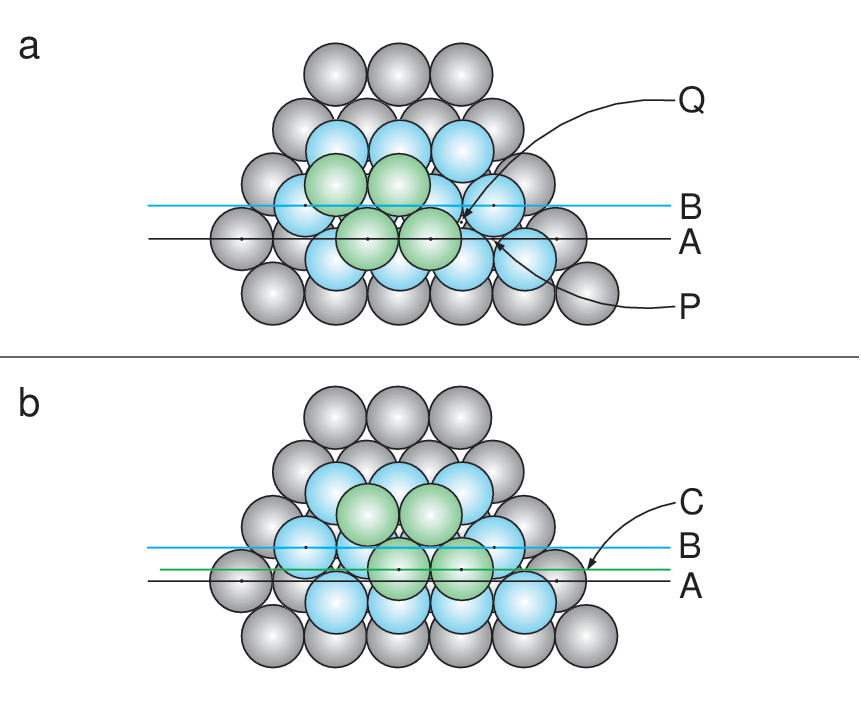
Legger man på ytterligere et slikt plan av kuler, kan de legges på to måter. Enten ligger kulene i det tredje planet rett over kulene i det første settet av kuler, eller så ligger de forskjøvet. Disse to formene er den tetteste måten å pakke like store kuler på. Den første måten kalles etter symmetrien for kubisk tetteste kulepakning og den andre kalles heksagonal tetteste kulepakning. I begge formene er hvert kule omgitt av 12 andre kuler i like stor avstand: seks i samme plan, tre i planet over og tre i planet under.
Slik er atomene i mange metaller ordnet på. Jern-, kobolt- og nikkel-atomer er pakket i en kubisk tetteste kulepakning. Magnesium, titan og kobolt er pakket i en heksgonal tetteste kulepakning.
I begge formene for kulepakning finnes det mindre hull med særlig enkel og symmetrisk form. Avhengig av symmetrien kalles de trigonale-, tetraeder- og oktederhull. Mindre atomer, som hydrogen og karbon fra fremstilling av disse metallene, kan ligge i disse hulrommene. Metallene vil da bli da sprø.
Metaller med heksagonal tetteste kulepakning er formbare (duktile), men oftest i mindre grad enn metaller med kubisk tetteste kulepakning. Også strukturen av noen enkle salter kan beskrives på grunnlag av en form for tetteste kulepakning. Det gjelder blant annet wurtzitt, ZnS, hvor svovelatomene er pakket som i kubisk tetteste kulepakning og sinkatomen er lokalisert i halvparten av de hulrommene som har tetraedriske omgivelser.




Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.